Weltweit ist der Bedarf an Organen viel höher als Spenderorgane zur Verfügung stehen. Allein in Deutschland stehen derzeit rund 8.500 Menschen auf der Warteliste für ein Organ. Um dieser Herausforderung zu begegnen, die Wartezeiten für Transplantationspatientinnen und -patienten zu verkürzen und mehr Organe verfügbar zu machen, forschen Medizinerinnen und Mediziner bereits an verschiedenen Lösungen. Neben einer Änderung der gesetzlichen Grundlagen für eine Organspende – unter anderem Widerspruchslösung, Organspende nach Herztod – stellt die sogenannte Maschinenperfusion ein vielversprechendes Verfahren zur Verbesserung der aktuellen Situation dar. Im Interview mit aachener FORSCHUNG erklärt Univ.-Prof. Dr. med. Florian Vondran, Direktor der Klinik für Allgemein-, Viszeral-, Kinder- und Transplantationschirurgie an der Uniklinik RWTH Aachen, die Anwendung der maschinellen Organperfusion, wo sie bereits zum Einsatz kommt und welche Chancen sich damit für die Transplantationsmedizin eröffnen.
Herr Prof. Vondran, wie sieht die Organspende-Situation aktuell aus?
Prof. Vondran: Die Transplantation ist eine etablierte Therapie und oftmals einzige Möglichkeit der Behandlung oder gar Rettung für Menschen, deren Organe wie Herz, Leber, Niere oder Lunge versagen. Die Zahl der Organspenderinnen und -spender ist jedoch hierzulande seit jeher deutlich zu niedrig, um allen Patientinnen und Patienten, die sich auf den Wartelisten befinden und auf ein Spenderorgan hoffen, zu helfen. Infolgedessen verschlechtert sich ihr Gesundheitszustand oft erheblich. Viele von ihnen versterben, während sie verzweifelt auf ein neues Organ warten.
Woran liegt das?
Prof. Vondran: Die Gründe sind vielfältig: Zum Beispiel ist die Organspende in Deutschland – anders als in den meisten anderen europäischen Ländern – nach der Entscheidungslösung geregelt. Das bedeutet, die Entnahme von Organen nach dem Tod ist nur zulässig, wenn die verstorbene Person dem zu Lebzeiten oder stellvertretend die Angehörigen aktiv zugestimmt haben. Doch nur gut ein Drittel aller Deutschen besitzt überhaupt einen Organspendeausweis. Aufgrund der geringen Spendebereitschaft und der immer älter werdenden Organspender nimmt auch die Qualität der Spenderorgane stetig ab und die Transplantationsmediziner sind zunehmend gezwungen, auch bereits vorgeschädigte Organe zu verwenden. Diese sogenannten marginalen Organe reagieren besonders sensibel auf die unzureichende Sauerstoff- und Nährstoffversorgung während der Entnahme aus dem Körper des Spendenden, der Aufbewahrung bis zum Zeitpunkt der Transplantation und der eigentlichen Transplantation selbst, was letztlich zu einem erhöhten Komplikationsrisiko für den Empfangenden führt. Häufig findet eine Transplantation dieser potentiellen Transplantate aufgrund des Risikos, dass die Organe nach der Transplantation nicht oder nur eingeschränkt funktionieren, gar nicht erst statt. Vor diesem Hintergrund gibt es derzeit nur die Möglichkeit, neue Wege zu beschreiten, um die Qualität und die Anzahl der zur Verfügung stehenden Spenderorgane zu erhöhen. Die sogenannte Maschinenperfusion von entnommenen Organen eröffnet der Transplantationsmedizin und vor allem ihren Patientinnen und Patienten neue Chancen und Perspektiven.
Was können wir uns unter Maschinenperfusion vorstellen?
Prof. Vondran: Bereits seit vielen Jahren beschäftige ich mich im Rahmen experimenteller und klinischer Studien mit der Verbesserung der Transplantabilität von Organen mit erhöhtem Risiko in der Nieren- und Lebertransplantation. Die Maschinenperfusion ist eine Technik, die bereits ganz zu Beginn der Transplantationschirurgie eingesetzt wurde, in den folgenden Jahrzehnten aber aufgrund der Einfachheit dieses Verfahrens durch die statische Kaltlagerung der Organe verdrängt wurde. Seit etwa 15 Jahren wird diese Technik aufgrund der zunehmenden Notwendigkeit, auch vorgeschädigte Organe zu transplantieren, wieder vermehrt angewandt. Bei diesen Organen hat man inzwischen gelernt, dass die einfache Kaltlagerung an ihre Grenzen stößt. Mithilfe der Maschinenperfusion können auch Spenderlebern erfolgreich transplantiert werden, die bisher aufgrund ihrer Qualität oder Lagerungszeit nicht oder nur unter deutlich erhöhtem Risiko verwendet werden konnten. Dabei wird die entnommene Spenderleber nach der Organentnahme und noch vor der Transplantation, also außerhalb des Körpers („ex vivo“), an eine Pumpe angeschlossen, kontinuierlich entweder mit Konservierungslösungen oder Blut perfundiert und „rekonditioniert“. Hierdurch werden zum Beispiel die Energiespeicher der Zellen wieder aufgeladen.
Wie können wir uns das konkret vorstellen?
Prof. Vondran: Grundsätzlich unterscheidet man im Rahmen der Maschinenperfusion zwei verschiedene Ansätze: Die hypotherme („kalte“) und die normotherme („warme“) Perfusion. Im Rahmen der hypothermen Perfusion wird eine mit Sauerstoff angereicherte, acht bis zehn Grad kalte Konservierungslösung kontinuierlich durch das Organ gepumpt. Im Rahmen der Lebertransplantation erfolgt dies über eine Dauer von bis zu vier Stunden, häufig parallel zur Entfernung der kranken Leber des Empfangenden. Der Vorteil ist hierbei, dass der Energieverbrauch des Transplantats gedrosselt wird und schädliche Moleküle aus dem Organ gespült werden, die im Rahmen der Lagerung auf Eis entstehen. Zusätzlich verbessert die Sauerstoffzufuhr den Stoffwechsel der Mitochondrien, welche als „Kraftwerke“ der Zellen eine besondere Rolle im Rahmen dieser Mangelversorgung einnehmen. Mit dieser Technik können wir somit Vorschäden sowie die Schädigung der Leber zwischen Entnahme und Transplantation erheblich reduzieren und auf diese Weise die Funktion des Organs beim Empfänger verbessern.
Bei der normothermen Maschinenperfusion hingegen wird statt einer kalten Konservierungslösung eine Lösung angewandt, die Blut (Erythrozytenkonzentrate) als Sauerstoffträger enthält. Die Perfusion erfolgt hierbei unter nahezu physiologischen Temperatur- (circa 36 Grad Celsius) und Blutdruckbedingungen. Die perfundierten Organe können so theoretisch mehrere Tage außerhalb des Körpers „überleben“. Zusätzlich besteht die Möglichkeit, die Funktion des Organs zu überprüfen. Auf diese Art werden beispielsweise Lebern identifiziert, die früher aufgrund schlechter Werte im Spendenden nicht transplantiert worden wären und nun erfolgreich für die Transplantation eingesetzt werden können. In der experimentellen Forschung liegt darüber hinaus ein Fokus auf der Reparatur oder Modifikation marginaler Organe, um ihre Qualität zu verbessern oder ihre Immunogenität zu reduzieren.
Insgesamt lässt sich somit festhalten, dass die maschinelle Perfusion von Spenderorganen verglichen mit der herkömmlichen kalten Lagerung auf Eis eine Vorbehandlung erlaubt, welche die Sicherheit für den Empfänger oder die Empfängerin eines Transplantates klinisch relevant erhöht.
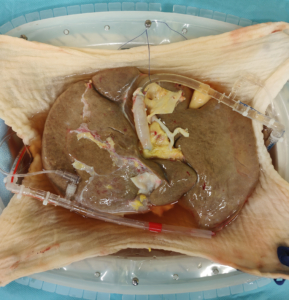
Eine Spenderleber, die mittels hypothermer oxygenierter Perfusion (HOPE) behandelt wird.
Wie erfolgt die Prüfung der Organfunktion bei der Maschinenperfusion?
Prof. Vondran: Im Rahmen der hypothermen Maschinenperfusion ist dies nur sehr begrenzt möglich. Ein Ansatz ist, Abbauprodukte des Zellstoffwechsels, die bei Schädigung der Zellen freigesetzt werden, als Surrogatparameter für eine ausreichende Organfunktion zu messen. Die normotherme Maschinenperfusion erlaubt durch die Aufnahme des Stoffwechsels während der Perfusion die Überprüfung konventioneller Parameter wie beispielsweise der Galleproduktion oder des Zuckerstoffwechsels.
Sie nannten als Beispiel die Spenderleber. Für welche anderen Organe kommt dieser Behandlungsansatz aktuell und in Zukunft noch infrage?
Prof. Vondran: Prinzipiell profitieren alle transplantierbaren Organe von den genannten Perfusionstechniken, wenngleich unterschiedliche Organe eine andere Toleranz für die mangelnde Versorgung mit Sauerstoff oder Nährstoffen aufweisen. Das Herz oder die Lunge haben beispielsweise eine äußerst geringe Ischämietoleranz, entsprechend wird die Maschinenperfusion auch hier bereits eingesetzt. Darüber hinaus besteht eine große Hoffnung, vorgeschädigte Organe mit der Maschinenperfusion nicht nur besser konservieren, sondern in der Zukunft auch reparieren oder modifizieren zu können, sodass die Organe länger und besser im Empfangenden funktionieren.
Wie schätzen Sie die Bedeutung der Perfusion in der Transplantationsmedizin ein?
Prof. Vondran: Verbesserte Organqualität und Therapieergebnisse, weniger Organverluste, höhere Patientensicherheit und ein erweiterter Spenderpool: Diese Vorteile verspricht die maschinelle Technik zur Organkonservierung. Entsprechend hat sich die Maschinenperfusion von Spenderorganen in den letzten Jahren gleich in mehreren klinischen Studien als effektives und sicheres Verfahren erwiesen. Die Uniklinik RWTH Aachen ist eines der ersten Transplantationszentren in Deutschland, das dieses Verfahren im Rahmen einer randomisierten klinischen Studie angewendet hat. Diese technologische Entwicklung gilt als Meilenstein der Transplantationsmedizin. Durch die Möglichkeit der Aufbereitung können auch zunehmend Spenderorgane genutzt werden, die bislang als unbrauchbar abgelehnt werden mussten. Das maschinelle Perfusionsverfahren hat somit auf lange Sicht großes Potential zur Verminderung des Organmangels und zur Steigerung der Transplantationsrate, was letztlich mit einer Reduktion der Sterblichkeit auf der Warteliste einhergeht.
In Deutschland wird die Technik bereits an mehreren Transplantationszentren eingesetzt, ist aber noch nicht als genereller Standard implementiert. Anders an der Uniklinik RWTH Aachen: Hier haben wir die (hypotherme) Maschinenperfusion als klinischen Standard bei der Lebertransplantation erfolgreich etabliert.
Wann kann diese Technik zum flächendeckenden Standardverfahren in der Organtransplantation werden? Welche Voraussetzungen sind dafür erforderlich?
Prof. Vondran: Wie so oft wird die Finanzierung der Verfahren durch die Kostenträger von entscheidender Bedeutung sein. Hierfür müssen wir als Behandelnde und Forschende die wissenschaftliche Evidenz ausbauen, damit klar wird, dass unser Gesundheitssystem von einer flächendeckenden Anwendung profitiert. Darüber hinaus liegen für einige Organe bereits Daten vor, die zeigen, dass die Maschinenperfusion bereits im Rahmen der Organspende im Spenderkrankenhaus und nicht erst vor Ort im Transplantationszentrum eingesetzt werden sollte. So plant die Deutsche Stiftung Organtransplantation (DSO), die die Organspende in Deutschland koordiniert, die hypotherme Maschinenperfusion als Standard bei der Nierenspende unmittelbar nach der Organentnahme einzuführen. Das wird die Organqualität in erheblichem Maße verbessern. Wir sehen Evidenz, dies auch für die Lebertransplantation zu etablieren. Auch hier spielt natürlich die Finanzierung eine erhebliche Rolle.
Bedarf es noch weiterer Forschung? Sind weitere Studien geplant?
Prof. Vondran: Es besteht bereits jetzt kein Zweifel daran, dass die Maschinenperfusion die Behandlungsqualität im Bereich der Transplantationsmedizin verbessert. Es gibt allerdings noch reichlich Forschungsbedarf. Unter anderem, welche Art von Maschinenperfusion, in welcher Situation und für welches Organ die besten Ergebnisse liefert. Darüber hinaus bestehen in der experimentellen und translationalen Forschung zahlreiche Fragestellungen, die auch wir in der Uniklinik RWTH Aachen bearbeiten. Unter anderem wollen wir die oben erwähnten Schädigungen im Rahmen der Lebertransplantation durch zusätzliche Maßnahmen während der Maschinenperfusion weiter eindämmen. Auch die genetische Modifikation von Organen während der normothermen Maschinenperfusion, um diese beispielweise immunologisch „unsichtbar“ zu machen, ist ein vielversprechender Forschungsansatz, um in Zukunft gegebenenfalls ganz auf die sonst lebenslang notwendige Immunsuppression verzichten zu können.
Wenn Sie einen Blick in die Zukunft wagen, wie wird sich die Transplantationsmedizin in den nächsten Jahrzehnten entwickeln?
Prof. Vondran: Ich denke, wir stehen vor einer spannenden Zeit in der Transplantationsmedizin. Nach Jahren des Stillstands gibt es mit der Maschinenperfusion eine Technologie, mit der wir Behandelnde und Forschende nicht mehr nur auf gesellschaftspolitische Lösungen angewiesen sind, sondern durch Innovationen den Pool an Organen selbst erweitern können. Auch auf dem Gebiet der Xenotransplantation, also der Verwendung von gentechnisch veränderten Organen von Tieren wie Schweinen, gibt es aktuell echte Fortschritte, wie jüngste Berichte aus den USA zeigen. Unsere Klinik will diese spannenden Prozesse aktiv mitgestalten. ![]()