Wissenschaftler der Uniklinik RWTH Aachen, des Deutschen Krebsforschungszentrums (DKFZ), des Deutschen Konsortiums für Translationale Krebsforschung (DKTK) und des Nationalen Centrums für Tumorerkrankungen (NCT) Heidelberg entwickeln eine Computer-basierte Methode zur verbesserten Therapiesteuerung von Patientinnen und Patienten mit Krebserkrankungen des Magen-Darm-Traktes. Die Ergebnisse dieser Arbeit wurden nun im renommierten Wissenschaftsjournal Nature Medicine publiziert.
Die Möglichkeiten, die sich durch die Anwendung von künstlicher Intelligenz (KI) und sogenanntem Maschinenlernen bieten, werden zukünftig zu einer fundamentalen Wandlung unseres Alltagslebens führen, was bereits als zweite digitale Revolution bezeichnet wird. Auch in der Medizin könnten computergestützte Verfahren zukünftig neue Möglichkeiten bieten, Patientinnen und Patienten zukünftig besser und zielgerichteter zu behandeln.
In den letzten Jahren wurde eine neue Therapieform gegen Krebs entwickelt, bei der durch neue Medikamente bei bestimmten Krebsarten wie Lungenkrebs oder schwarzem Hautkrebs (Melanom) das Immunsystem zur Krebsbekämpfung stimuliert werden kann. Klinische Studien zeigten, dass bei Krebserkrankungen des Magen-Darm-Traktes, zum Beispiel bei Darmkrebs oder Magenkrebs, diese Immuntherapie aber nur bei einer bestimmten Untergruppe von Patienten sinnvoll anwendbar wäre, bei denen ein bestimmtes genetisches Merkmal im Tumor vorliegt, die sogenannte Mikrosatelliten-Instabilität.
„Bisher sind zusätzliche genetische Tests an Tumorproben notwendig, um zu erkennen, ob eine Mikrosatelliten-Instabilität vorliegt und damit eine Immuntherapie bei Darmkrebspatienten besonders gut wirken könnte“, sagt Dr. med. Jakob Nikolas Kather, Arzt und Wissenschaftler an der Uniklinik RWTH Aachen und Mitarbeiter am DKFZ und am Nationalen Centrum für Tumorerkrankungen Heidelberg. „Wir haben daher eine Methode entwickelt, mit der wir mit Hilfe von ‚Deep Learning‘ – einer Form des auf künstlicher Intelligenz beruhenden Maschinenlernens – ein Computerprogramm trainieren können, dieses wichtige Merkmal direkt an einer kleinen Tumorprobe und ohne weitere genetische Tests zu erkennen.“
Ein solches Verfahren könnte zukünftig die Testung auf bestimmte Eigenschaften eines bösartigen Tumors deutlich vereinfachen und so langfristig dazu beitragen, dass mehr Krebspatientinnen und -patienten Zugang zu einer an ihre speziellen Bedürfnisse angepassten, optimalen Therapie bekommen. „Bevor eine breite Anwendung für Patientinnen und Patienten in der Zukunft möglich ist, müssen die Ergebnisse der aktuellen Studie allerdings zunächst in weiteren, größeren Untersuchungen bestätigt werden“, sagt Univ.-Prof. Dr. med. Tom Lüdde, Leitender Oberarzt und beteiligter Wissenschaftler aus der Klinik für Gastroenterologie, Stoffwechselerkrankungen und Internistische Intensivmedizin (Medizinische Klinik III) der Uniklinik RWTH Aachen, dessen Forschungsarbeit an der Uniklinik RWTH Aachen unter anderem durch eine Mildred-Scheel-Stiftungsprofessur der Deutschen Krebshilfe unterstützt wird.
Die RWTH Aachen University sowie die Uniklinik RWTH Aachen haben es zu ihrem Schwerpunkt erklärt, die mögliche Anwendung und die Chancen neuer digitaler Techniken für Patientinnen und Patienten in der Zukunft zu erforschen und ihre Vorreiterrolle im Bereich Medizin und Technik weiter auszubauen. „Dabei werden wir aber die Sorgen und ethischen Bedenken, die mit diesen neuen Methoden verbunden sind, nicht aus dem Blick verlieren und die menschlichen Bedürfnisse unserer Patientinnen und Patienten auch weiterhin ins Zentrum unseres täglichen Handelns stellen“, versichert Univ.-Prof. Dr. rer. nat. Stefan Uhlig, Dekan der Medizinischen Fakultät und Vorstandsmitglied der Uniklinik RWTH Aachen.
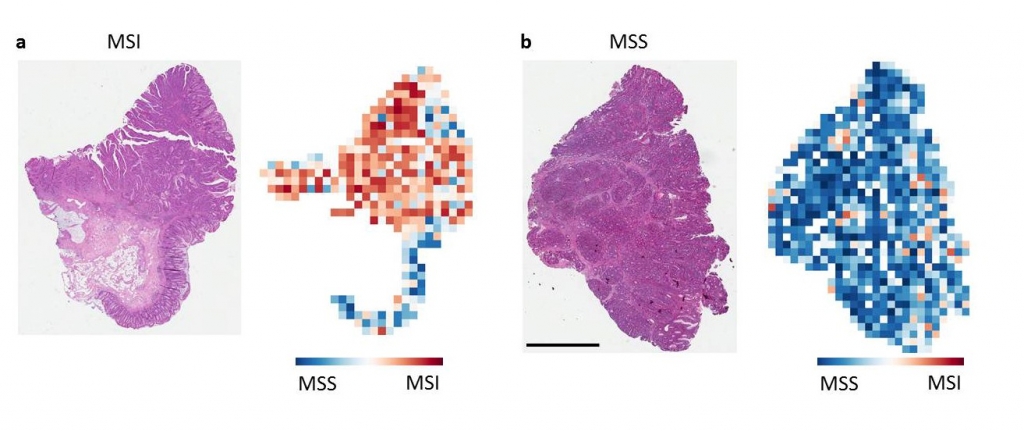
Gewebeschnitte von einem Mikrosatelliten-instabilen (MSI) Patienten (a) und einem Mikrosatelliten-stabilen (MSS)-Patienten.
Originalpublikation
Jakob Nikolas Kather, Alexander T. Pearson, Niels Halama, Dirk Jäger, Jeremias Krause, Sven H. Loosen, Alexander Marx, Peter Boor, Frank Tacke, Ulf Peter Neumann, Heike I. Grabsch, Takaki Yoshikawa, Hermann Brenner, Jenny Chang-Claude, Michael Hoffmeister, Christian Trautwein, Tom Luedde (2019) Deep learning can predict microsatellite instability directly from histology in gastrointestinal cancer. Nature Medicine, https://doi.org/10.1038/s41591-019-0462-y ![]()